順天堂大学大学院医学研究科乳腺腫瘍学講座の佐々木律子助教(写真)と齊藤光江教授、堀本義哉准教授、細胞・分子薬理学 呉林なごみ客員准教授、難病の診断と治療研究センター 江口英孝先任准教授、ゲノム・再生医療センター 赤松和土教授、循環器内科 宮崎彩記子特任准教授らのグループは乳がん患者の末梢血T細胞からiPS細胞を樹立して心筋細胞を誘導、トラスツズマブ誘発性重症心毒性の発症機序を研究する方法を確立した。樹立した心筋細胞モデルの機能解析や網羅的遺伝子解析の結果、トラスツズマブによる重篤な心毒性発症には、KLK5-PAR2-MAPK経路を介した炎症シグナル亢進がかかわっている可能性が明らかになった。この結果は専門誌Cancer Science(2022年7月25日発行)と第30回日本乳癌学会学術総会(2022年6月30日~7月2日)で報告された。
トラスツズマブはHER2抗原(ErbB2)を標的とする抗体医薬で、HER2過剰発現が確認された乳がん、胃がん、唾液腺がんに適応をもつ。副作用として注目されているのが心毒性で、佐々木助教は「5~10%の頻度で左室機能不全を発症する。年齢、高血圧、心血管疾患の既往、抗がん剤治療投与歴など心毒性発症リスク因子が報告されているが、リスクに乏しい患者においても、しばしば経験される。非蓄積性で発症機序が不明な点が多く、発症予測も困難であることから治療の障壁になることがある」と指摘する。
ErbBシグナル経路は正常な心筋においても存在しており、ストレスがかかった状況下で活性化され心保護的な役割を担っているとされている。先行研究ではErbB2シグナル経路阻害による心筋細胞の細胞内エネルギー代謝障害の発生などが指摘されているが、本質に迫るには程遠い状況だ。佐々木助教らの着眼点は「なぜ心毒性を発症する人と発症しない人がいるのか」というものだ。この個人差が出現する原因を探れば、トラスツズマブ誘発性心毒性全体の発症機序に迫ることができると考えた。
佐々木助教は、トラスツズマブの治療を受けた乳がん患者のうち、左室駆出率が治療前のベースラインと比較して30%以上低下した低リスクの重篤な心毒性患者群を「SP群」、各種パラメーターでマッチングした未発症患者群を「NP群」(投与後1年以上心機能低下を発症しなかった症例)と規定した。それぞれの患者群の末梢T細胞リンパ球からiPS細胞を誘導、さらに心筋細胞へと分化させた。順天堂医院で2010年から2019年のトラスツズマブ投与を受けた症例(n=468)からSP群(n=10、2.1%)とNP群(n=444、94.9%)を選び、それぞれ3例ずつの心筋細胞を作製した。治療前に施行した心臓超音波で測定した心筋機能評価パラメーターにはSP群、NP群の両患者群間で違いはなく、異常がないことが確認されている。
SP群の心筋細胞モデルでは炎症シグナル亢進が認められる
トラスツズマブを添加した培地で患者由来iPS細胞由来心筋細胞を1週間培養するとSP群のほうで顕著な心収縮・弛緩速度の低下が認められた。またSP群ではATP産生量低下、オートファジー活性の低下、活性酸素種の蓄積増加なども確認できた。つまり、このモデルがトラスツズマブ感受性の心筋細胞の機能を再現できるものであることが明らかになった。
次に佐々木助教らはSP群とNP群のRNAシークエンスを行った。両群間で発現の相違を認めた遺伝子を抽出、さらにその中から既報で心毒性に関与する遺伝子を選択し、定量的逆転写PCR検査(qRT-PCR)を行った。さらにqRT-PCRでも発現に違いが認められた遺伝子のなかでトラスツズマブ投与前からSP群で発現が亢進していたセリンプロテアーゼ関連遺伝子とトラスツズマブ投与後にSP群で高発現していた炎症関連遺伝子を対象に解析を進めた。
その結果、SP群では培地上清からカリクレイン関連ペプチダーゼ(KLK)5とKLK8が検出された。さらにKLK5シグナルの下流に位置するプロテアーゼ受容体(PAR-2)はNP群よりもSP群で発現量、活性化が高値であった。さらに、PAR-2受容体アンタゴニスト(I-191、FSLLRY-NH2)によりトラスツズマブ投与で増加したmRNA IL-1βが抑制されることが示された。
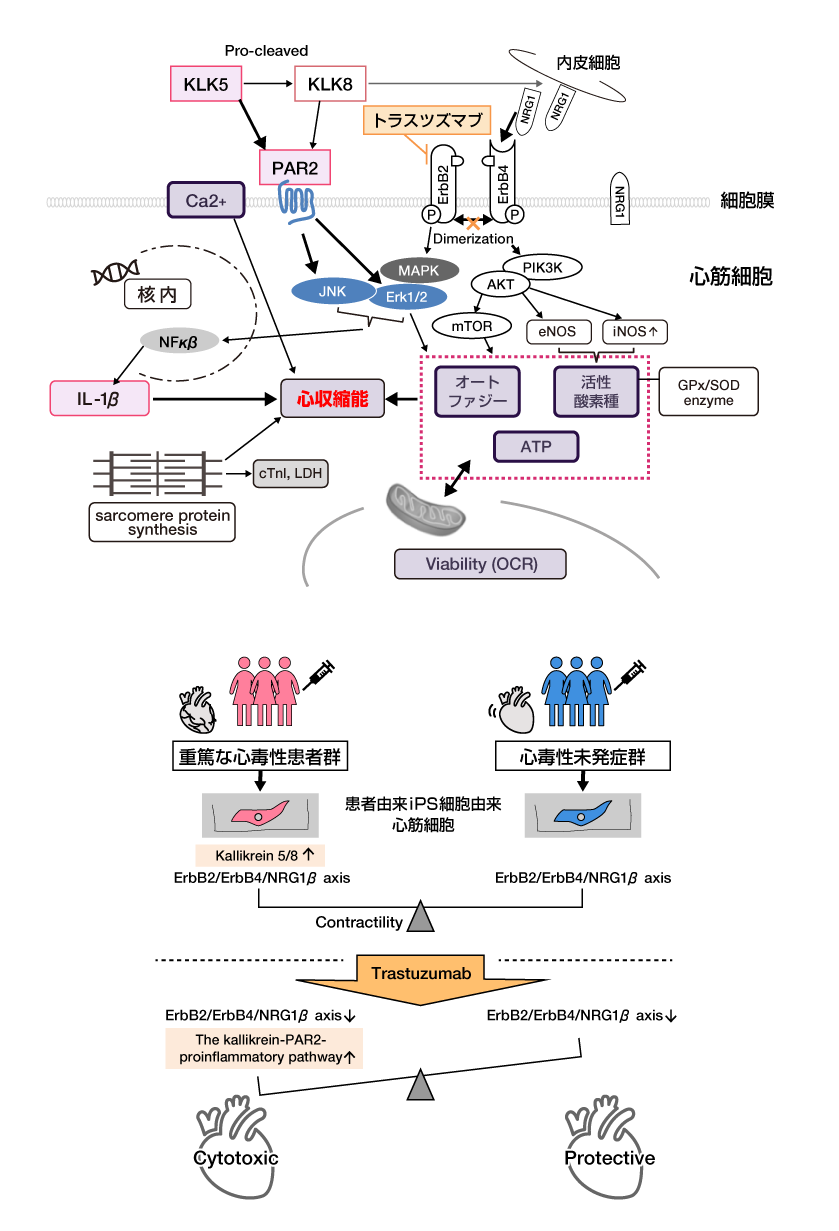
以上の結果から、佐々木助教らはトラスツズマブ心毒性の発生機序を以下のように推察する(図)。
「心毒性を発症したSP群ではKLK5-PAR2-MAPK経路を介した炎症シグナル亢進がトラスツズマブの治療前から存在するが、HER2(ErbB2)シグナル経路が心毒性の発症を抑制している。そこで抗HER2療法によってHER2(ErbB2)シグナル経路が阻害された結果、炎症シグナルが相対的に強くなり、心毒性を発症する。」(佐々木助教)
今回の報告で、SP群とNP群とでは遺伝子発現パターンに違いがあることが明らかになった。この違いはどこから来るのか? 佐々木助教ら順天堂大学グループでは、SP群とNP群の全ゲノムシークエンスからその答を探る研究を開始しているという。
臨床応用へのシナリオ
これまでの研究結果について臨床応用の可能性はどうか。佐々木助教は「臨床応用の方法が2つ考えられる」と語った。1つは、心毒性誘発を早期に検知するバイオマーカーの探索だ。心不全の診断補助に用いる検査にはB型ナトリウム利尿ペプチド(BNP)、心筋トロポニンTやIがあるが、トラスツズマブ心毒性の早期診断には有用性が低いことが明らかになっている。佐々木助教が作成したSP群心筋モデル細胞にトラスツズマブを投与して培地に現れる成分の中には、こうした発症予測バイオマーカーとして使える成分がある可能性がある。
もう1つは、心毒性を予防する薬剤の探索だ。現在、トラスツズマブ心毒性が発症した場合にはアンジオテンシン変換酵素(ACE)阻害薬、アンジオテンシンII受容体拮抗薬(ARB)、アルドステロン拮抗薬、β遮断薬が用いられているが、モデル細胞から新しい治療薬の作用点がみつかる可能性がある。佐々木助教が報告したKLK5も有望な作用点の1つだ。
「現時点ではトラスツズマブ心毒性の発症を事前に予測する方法がない。有効な発症予測バイオマーカーがみつかり、さらに予防薬がみつかれば、ハイリスクの患者に事前に予防薬を投与することによってトラスツズマブの治療を中断することなく、治療が継続できるようになるはず」と佐々木助教は語っている。
図 推察されるトラスツズマブ心毒性の発生機序